|
|
 |
 |
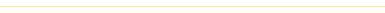 |
Substancje mogą występować w trzech podstawowych stanach skupienia: stałym, ciekłym i w postaci pary.
Gaz jest szczególnym stanem pary – takim, w którym pary nie można skroplić nawet przy użyciu bardzo dużych ciśnień. Nieraz jako czwarty stan skupienia podaje się plazmę – stan, w którym substancja jest całkowicie zjonizowana.
• Przemiany fazowe to procesy, w wyniku których substancje zmieniają swój stan skupienia. Schemat przedstawia wszystkie możliwe przemiany:

Parowanie nie jest przemianą fazową, gdyż nie zachodzi w stałej dla danej substancji temperaturze przemiany, lecz w każdej temperaturze.
• Temperatura przemiany fazowej – stała temperatura, w której substancja zmienia stan skupienia.
Temperatura topnienia jest zawsze równa temperaturze krzepnięcia, zaś temperatura wrzenia jest równa temperaturze skraplania.
Stałość temperatury przemiany fazowej dotyczy bez wyjątku wszystkich substancji o tak zwanej budowie krystalicznej. Wyjątkiem są takie substancje, jak szkło lub żywice, których temperatura zmienia się w trakcie zmiany fazy. Substancje takie nazywa się ciałami bezpostaciowymi.
|
|
|
 |
|
 |
|
|

